Le DPI ou diagnostic génétique préimplantatoire est une technique utilisée en procréation assistée pour s'assurer que les embryons qui sont transférés dans l'utérus sont exempts d'altérations génétiques, qu'il s'agisse de maladies héréditaires ou d'anomalies chromosomiques.
Le DPI est réalisé au cours d'un traitement de fécondation in vitro (FIV), lorsque les embryons ont été mis en culture pendant 3 à 5 jours et qu'il est possible de réaliser une biopsie des blastomères.
Les indications du DPI sont, d'une part, le risque de transmission de maladies héréditaires d'un ou des deux parents ou, d'autre part, lorsque les ovules et les spermatozoïdes sont de mauvaise qualité et peuvent accumuler des mutations dans leur ADN.
Vous trouverez ci-dessous un index des 8 points que nous allons aborder dans cet article.
- 1.
- 2.
- 2.1.
- 2.2.
- 2.3.
- 2.4.
- 2.5.
- 3.
- 3.1.
- 3.2.
- 4.
- 4.1.
- 4.2.
- 4.3.
- 4.4.
- 4.5.
- 4.6.
- 5.
- 6.
- 7.
- 8.
Indications
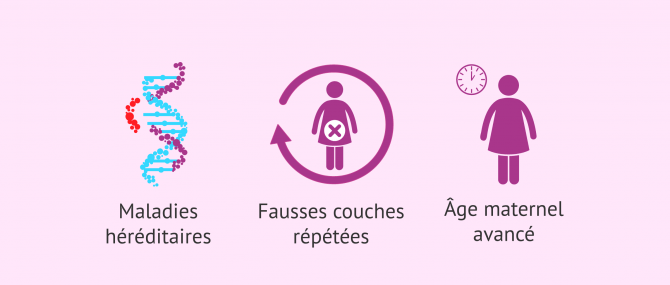
Le DPI permet de détecter les embryons présentant des altérations dans leur séquence d'ADN qui peuvent conduire à des fausses couches ou, pire encore, à la naissance d'enfants malades.
Beaucoup de ces maladies sont héréditaires, c'est-à-dire qu'elles sont transmises par les familles. Ainsi, un couple qui souffre d'une altération génétique ou qui se sait porteur peut être assuré d'avoir un enfant sain grâce à cette méthode.
D'autres anomalies génétiques, en revanche, apparaissent de novo dans les embryons après la fécondation. Dans ce cas, l'indication du DPI se pose lorsque la femme a subi des fausses couches à répétition ou si elle est d'un âge maternel avancé.
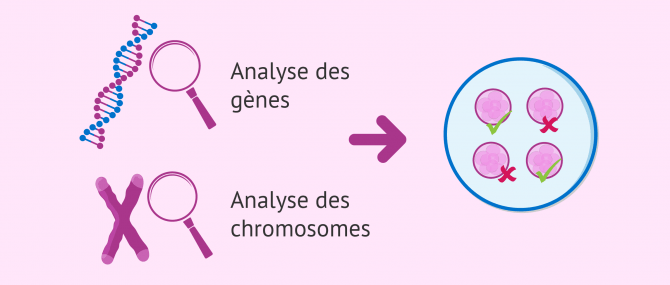
Au cours d'un traitement de FIV avec DPI, après l'obtention des résultats, les embryons diagnostiqués avec l'altération génétique sont éliminés. Seuls les embryons sains et exempts de mutations seront transférés dans l'utérus maternel ou vitrifiés pour une utilisation ultérieure.
Le diagnostic génétique préimplantatoire a permis la naissance de milliers d'enfants exempts de maladies génétiques dans le monde entier et, en outre, c'est une technique approuvée par la loi 14/2006 en Espagne.
La PMA, comme tout traitement médical, exige que vous fassiez confiance au professionnalisme des médecins et de la clinique que vous avez choisis. Évidemment, tous ne sont pas identiques. Le Rapport sur la fertilité sélectionne les cliniques les plus avantageuses pour vous selon nos critères de qualité rigoureux. De plus, le système effectue une comparaison des prix et des conditions offertes par les différentes cliniques afin de faciliter votre prise de décision.
Enfin, il convient de noter que les altérations de l'ADN d'un être humain peuvent être différenciées:
- Altérations génétiques
- affectent un ou plusieurs gènes.
- Altérations chromosomiques
- affectent un ou plusieurs chromosomes.
Le Dr Antonio Alcaide, embryologiste spécialiste du DPI, explique les particularités de ce processus:
Actuellement, le DPI peut être utilisé par les couples qui n'obtiennent pas de grossesse après le transfert de plusieurs embryons de bonne qualité, les couples qui font des fausses couches à répétition, les couples âgés de plus de 38 ans et tous ceux qui sont porteurs ou affectés par une maladie génétique spécifique.
Tout au long de ce billet, nous aborderons chacun de ces types et donnerons des exemples des troubles les plus importants qui nécessitent un DPI.
Maladies d'origine génétique
Les maladies génétiques sont celles causées par la mutation du génome dans la séquence d'un seul gène (altérations monogéniques) ou de plusieurs gènes (altérations polygéniques).
En outre, si la mutation est présente dans les cellules germinales de l'être humain, c'est-à-dire dans les ovules et/ou le sperme, ces maladies seront transmissibles à la descendance.
La probabilité d'hériter d'une altération génétique dépend du type d'hérédité de chaque pathologie. C'est donc ainsi que sont classées les maladies d'origine génétique:
Autosomique dominant
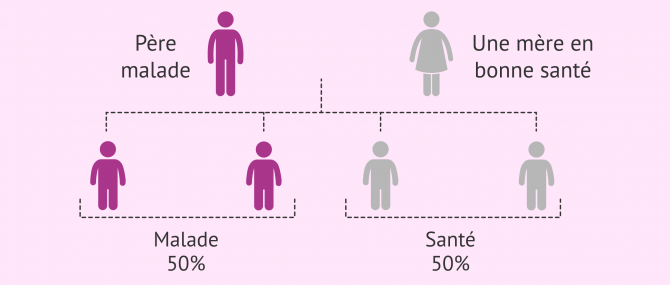
Ce sont les altérations qui affectent les chromosomes non sexuels. La personne contractera la maladie en héritant d'une seule copie du gène défectueux d'un parent, qui sera également malade.
La probabilité de transmettre la maladie d'un parent atteint à ses enfants est de 50 %.
Vous trouverez ci-dessous la liste des maladies autosomiques dominantes les plus caractéristiques:
- Achondroplasie
- Ataxie spinocérébelleuse SCA1 et SCA3
- Charcot-Marie-Tooth
- Dystrophie facio-scapulo-humérale
- Dystrophie myotonique (Steinert)
- La maladie d'Albers-Schomberg
- Sclérose tubéreuse de type 1
- Sclérose tubéreuse de type 2
- Exostoses multiples héréditaires
- Huntington
- Néoplasie endocrinienne multiple 1 et 2
- Neurofibromatose de types 1 et 2
- Ostéogenèse ou ostéogenèse imparfaite
- Paraparésie spastique familiale
- Maladie rénale polykystique, AD. Lié à la PKD1
- Maladie rénale polykystique, AD. Lié à la PKD2
- Polypose adénomateuse familiale
- Rétinite pigmentaire
- Syndrome de Lynch: cancer du côlon héréditaire et non polyposique
- Le syndrome de Marfan
- Syndrome de Noonan
- Syndrome de Von Hippel-Lindau
En raison de leur gravité et de leur forte probabilité de transmission à la descendance, la plupart de ces maladies ne nécessitent pas l'approbation de la Commission nationale de la procréation assistée (CNRHA) pour le DPI.
Autosomique récessif
De la même manière que dans le cas précédent, il s'agit d'altérations qui affectent les chromosomes non sexuels. Au contraire, pour qu'une personne soit atteinte de la maladie, elle doit hériter des deux copies du gène défectueux, l'une du père et l'autre de la mère.
Si vous héritez d'une copie normale et d'une copie défectueuse, vous ne serez que porteur de l'altération génétique. Les porteurs ne sont pas atteints de la maladie, mais ils ont la possibilité de la transmettre à leur progéniture.
La probabilité d'avoir un enfant malade si les parents sont porteurs est de 25 %, tandis qu'il y a 50 % de chances que l'enfant soit porteur de la mutation et seulement 25 % de chances que l'enfant naisse en parfaite santé.
Vous trouverez ci-dessous la liste des maladies autosomiques récessives les plus importantes:
- Acidurie glutarique de type 1
- Acidémie propionique A
- Acidémie propionique B
- L'anémie de Fanconi
- Ataxie de Friedreich
- Atrophie musculaire spinale (SMA)
- α-Thalassémie
- β-Thalassémie
- Défaut de glycosylation (CDG1A)
- Déficit en 21-Hydroxylase
- Déficience en L-CHAD
- Dysplasie hydrotique ectodermique (syndrome de Clouston)
- La maladie de Gaucher
- La mucoviscidose (CF)
- Gangliosidose
- Déficit immunitaire combiné sévère, alymphocytaire
- Leucodystrophie métachromatique
- Lymphohistiocytose familiale
- Mucopolysaccharidose IIIA (San Filippo A)
- Ostéopétrose infantile maligne
- Maladie rénale polykystique (ARPKD)
- Surdité neurosensorielle congénitale non syndromique
- Tyrosinémie de type 1
Dans ce cas, certaines de ces maladies nécessitent une autorisation préalable de la CNRHA pour procéder à un traitement de FIV par DPI. Toutefois, la grande majorité des demandes sont finalement approuvées.
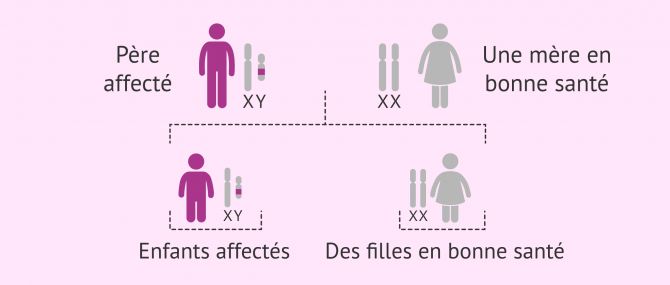
Dominante liée à l'X
Il s'agit de mutations qui affectent des gènes situés sur le chromosome sexuel X. Étant dominantes, ces maladies se manifestent à la fois chez les hommes et chez les femmes.
Les femmes malades ont 50 % de chances de transmettre la maladie à tous leurs enfants. Les hommes atteints, en revanche, le transmettront toujours à leurs filles, tandis que leurs fils seront sains.
Ce type d'héritage est très rare. Cependant, nous pouvons nommer les maladies dominantes liées à l'X suivantes:
- Incontinence pigmentaire
- Rachitisme hypophosphatémique
- Le syndrome de Fabry
- Syndrome de Rett
La fréquence de ces maladies est plus élevée chez les femmes que chez les hommes en raison du type d'hérédité. Toutefois, la gravité des symptômes est beaucoup plus importante chez les hommes, car ils ne possèdent qu'une seule copie du chromosome X.
Récessif lié à l'X
Il s'agit également de mutations qui affectent des gènes situés sur le chromosome sexuel X.
Étant récessives, il faudra qu'une femme hérite des deux copies défectueuses de ses parents pour avoir la maladie. Si elles n'héritent que d'une seule des copies, les femmes sont porteuses de ces maladies.
Toutefois, comme les hommes ne possèdent qu'un seul chromosome X, ils seront toujours atteints de la maladie même s'ils n'en reçoivent qu'une seule copie.
Parmi les maladies récessives liées au chromosome X, on trouve:
- Adrénoleucodystrophie
- Déficit en ornithine transcarbamylase
- Dystrophies musculaires de Duchenne et de Becker
- La maladie de Norrie
- Hémophilie
- Myopathie myotubulaire
- Mucopolysaccharidose I (syndrome de Hurler)
- Mucopolysaccharidose III (syndrome de Hunter)
- Syndrome d'Alport
- Le syndrome du X fragile
- Le syndrome de Lesch-Nyhan
En fonction de l'état de santé de chaque parent et du risque de transmission d'une maladie liée aux chromosomes sexuels, la sélection du sexe du futur bébé par DPI sera autorisée ou non, dans le but de ne pas transmettre la maladie.
Lié au chromosome Y
Il s'agit de mutations qui affectent les gènes situés sur le chromosome sexuel Y. Ce type d'hérédité est connu sous le nom d'hérédité holandrique.
Le chromosome Y n'étant présent que chez les hommes, tous les enfants mâles de parents atteints auront la maladie et risquent de la transmettre à leurs futurs enfants. Les femmes ne possèdent pas de chromosome Y. Elles ne seront donc jamais atteintes de la maladie.
Enfin, il est important de noter que les maladies génétiques liées au chromosome Y sont très rares. L'une des plus importantes est l'infertilité due aux microdélétions du chromosome Y.
Maladies chromosomiques
Les maladies chromosomiques, également appelées troubles chromosomiques, sont des maladies qui affectent le nombre ou la structure des chromosomes.
Comme pour les maladies génétiques, ces types d'anomalies peuvent être hérités. Cependant, elles peuvent également résulter d'une méiose défectueuse, entraînant des ovocytes ou des spermatozoïdes anormaux.
Il existe plusieurs causes de défauts de méiose: femmes de plus de 38 ans, traitements contre le cancer, médicaments, etc.
Certaines altérations chromosomiques sont compatibles avec la vie, donnant naissance à des individus présentant différents degrés d'implication en fonction du chromosome altéré. D'autres, en revanche, sont incompatibles avec la vie et donneront naissance à des embryons qui ne s'implanteront pas ou provoqueront des fausses couches à répétition.
Nous allons maintenant commenter les plus importantes:
Modifications numériques
La dotation chromosomique de l'être humain est de 46 chromosomes, 23 proviennent de la mère et 23 du père.
Les altérations du nombre de chromosomes présents dans chaque individu sont connues sous le nom d'aneuploïdie et il en existe les types suivants:
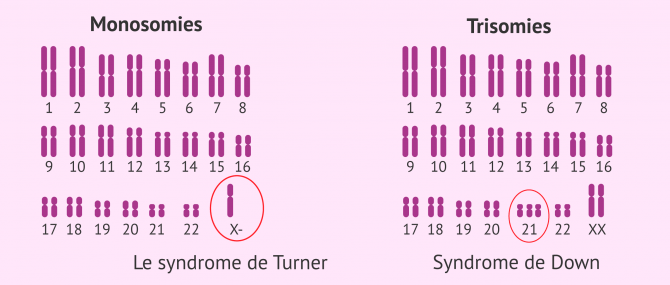
- Monosomies
- la personne a un chromosome en moins. Le cas le plus marquant est le syndrome de Turner, dans lequel la femme ne possède qu'un seul chromosome sexuel X (caryotype 45,X0).
- Trisomies
- la personne a un chromosome supplémentaire. Les exemples les plus fréquents sont les suivants : syndrome de Down (trois chromosomes 21), syndrome de Patau (trois chromosomes 13), syndrome d'Edwards (trois chromosomes 18), syndrome de Klinefelter (caryotype 47,XXY).
Si les chromosomopathies dont nous venons de parler sont compatibles avec la vie, d'autres, comme la trisomie 15 ou la trisomie 22, ne le sont pas.
Soixante pour cent des avortements du premier trimestre sont dus à une aneuploïdie, tout comme 6 % des mort-nés.
Modifications structurelles
Les altérations structurelles des chromosomes sont celles dans lesquelles il y a eu rupture et réarrangement de fragments chromosomiques.
Les types qui existent sont les suivants:
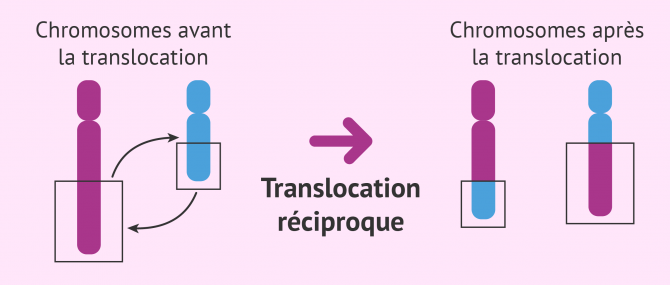
- Translocations
- transfert d'un fragment d'un chromosome à un autre. Les translocations peuvent être équilibrées, lorsque le changement de structure n'entraîne ni perte ni gain de matériel génétique, ou déséquilibrées, lorsqu'il y a perte ou gain d'ADN. Il existe également un type de translocation, la translocation robertsonienne, dans laquelle deux chromosomes acrocentriques fusionnent, qui comporte un risque de transmission de trisomies.
- Insertions
- un fragment de chromosome se déplace dans un autre chromosome.
- Investissements
- implique un réarrangement intrachromosomique, c'est-à-dire qu'un fragment de chromosome est inversé.
- Chromosome en anneau
- les extrémités du chromosome sont cassées et le chromosome circule. Elle a des effets graves car le chromosome affecté peut devenir inactif.
Vos questions fréquentes
Toutes les maladies peuvent-elles être diagnostiquées par une biopsie d'embryon?
La biopsie de l'embryon fournit des informations sur le patrimoine chromosomique ou la présence de certaines mutations (altérations des gènes). Cela nous permet d'établir un diagnostic précoce des maladies chromosomiques et de certaines maladies génétiques (celles qui sont connues et autorisées par la loi).
Cependant, cette technique ne permet pas de diagnostiquer toutes les maladies. Pour cette raison, il est très important d'effectuer un contrôle périnatal correct de la gestation et des enfants nés afin de diagnostiquer précocement d'autres types de maladies.
Lire la suite
Est-il conseillé d’effectuer un DPI dès qu’il y a un risque d'aneuploïdie?
Oui, c’est la seule technique qui permette de transférer dans l’utérus des embryons à dotation chromosomique normale, sans aneuploïdies chromosomiques.
Le syndrome de Klinefelter est-il une maladie génétique ?
Le syndrome de Klinefelter ou 47, XXY est une altération génétique qui se développe en raison de la séparation incorrecte des chromosomes homologues au cours de la méiose durant laquelle se produisent les gamètes de l'un des progéniteurs ou peut également se produire dans les premières divisions du zygote.
Les hommes atteints souffrent d'hypogonadisme hypergonadotrope, de gynécomastie, de difficultés d'apprentissage et d'infertilité. C'est la maladie génétique la plus répandue chez les hommes. Certains hommes ne présentent aucun symptôme et ne savent pas qu'ils souffrent de cette maladie jusqu'à l'âge adulte lorsqu'une stérilité survient.
Tous les embryons de qualité A sont-ils euploïdes?
La réponse est un non catégorique. Les embryons sont classés en différentes qualités en fonction de leur morphologie. Cependant, même si un embryon est de la plus haute qualité morphologique, nous ne pouvons pas garantir qu'il est chromosomiquement normal.
Il est vrai qu'il existe une certaine corrélation entre la qualité embryonnaire et l'euploïdie. Cette association est plus forte lorsque la qualité est évaluée au stade du blastocyste, puisque pendant les premiers jours, le développement embryonnaire dépend de l'énergie de l'ovocyte lui-même, alors qu'à partir du 2e ou 3e jour de développement, le génome embryonnaire est activé et le développement de l'embryon dépend largement de son propre matériel génétique.
Lire la suite
Peut-on faire un DPI pour éviter la trisomie 21 ?
Oui, dans le cas d'un âge avancé de la mère ou un trouble du caryotype, on peut réaliser un DPI pour éviter le syndrome dela trisomie 21. Cette maladie fait que l'embryon possède le chromosome 21 en triple exemple au lieu d'en avoir seulement deux (celui du père et celui de la mère).
Quelles maladies orphelines évitent le DPI ?
Tout dépend de la fréquence d'apparition de la maladie génétique dans une zone géographique concrète. En France, on a recours au DPI pour éviter les maladies comme le syndrome X-fragile, la maladie de Huntington ou la myopathie.
La rédaction vous recommande
Si vous souhaitez savoir comment se déroule le traitement de la FIV avec le DPI étape par étape, nous vous invitons à poursuivre votre lecture dans le post suivant: Quelle est la procédure de diagnostic génétique préimplantatoire (DPI)?
Communauté et Soutien
Chez inviTRA nous travaillons pour rendre l'information mensuelle et rigoureuse accessible à tous. Si cet article vous a aidé, envisagez de nous soutenir afin que nous puissions continuer à accompagner davantage de personnes dans leur chemin vers la parentalité.
Bibliographie
Angell, R.R., Xian, J and Keith, J. (1993) Chromosome anomalies in human oocytes in relation to age. Hum. Reprod., 8, 1047–1054.
Buster, J.E. and Carson, S.A. (1989) Genetic diagnosis of the preimplantation embryo. Am. J. Med. Genet., 34, 211–216.
Delhanty, J.D.A. and Handyside, A.H. (1995) The origin of genetic defects in the human and their detection in the preimplantation embryo. Hum. Reprod. Update, 1, 201–215.
Florensa, M. (2011). Diagnóstico genético preimplantacional para enfermedades de aparición tardía. Rev. Asoc. Est. Biol. Rep., Vol. 16, Nº 1, pág. 45-46.
Genetic Alliance; District of Columbia Department of Health. Understanding Genetics: A District of Columbia Guide for Patients and Health Professionals. Washington (DC): Genetic Alliance; 2010 Feb 17. Appendix H, Chromosomal Abnormalities.
Genetics Home Reference (Nov 7, 2018). Inheriting Genetic Conditions. In: Help Me Understand Genetics. Lister Hill National Center for Biomedical Communications U.S. National Library of Medicine National Institutes of Health Department of Health & Human Services.
Harper, J.C. (1996) Preimplantation diagnosis of inherited diseases by embryo biopsy: an update of the world figures. J. Assist. Reprod. Genet., 11, 132–143.
Mastenbroek S, Twisk M, van Echten-Arends J, Sikkema-Raddatz B, Korevaar JC, Verhoeve HR, Vogel NE, Arts EG, de Vries JW, Bossuyt PM et al. (2007). In vitro fertilization with preimplantation genetic screening. N Engl J Med; 357: 9– 17.
Vos questions fréquentes: 'Toutes les maladies peuvent-elles être diagnostiquées par une biopsie d'embryon?', 'Est-il conseillé d’effectuer un DPI dès qu’il y a un risque d'aneuploïdie?', 'Peut-il y avoir une trisomie 21 malgré le DPI?', 'Le syndrome de Klinefelter est-il une maladie génétique ?', 'Tous les embryons de qualité A sont-ils euploïdes?', 'Peut-on faire un DPI pour éviter la trisomie 21 ?' et 'Quelles maladies orphelines évitent le DPI ?'.
Auteurs et collaborateurs




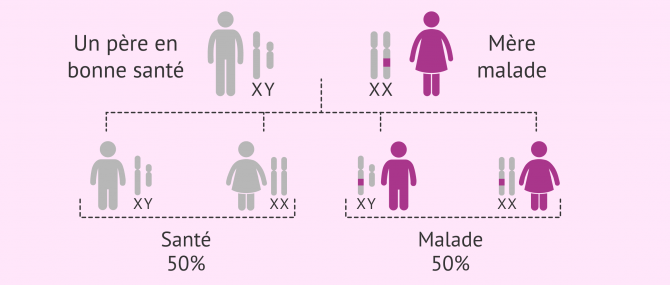
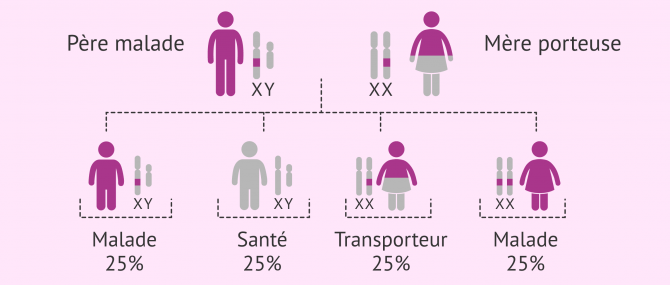



Je ne l’avais pas inscrit sur le commentaire précédent, mais mon compagnon est atteint également d’une maladie le syndrome d »Ehlres Danlos. Je me demandais si également elle serait détectée avec une DPI ? merci
Bonjour,
Je suis atteinte d’une dermatomyosite juvénile et mon compagnon et moi nous voulons fonder une famille, sauriez-vous me dire si la DPI pourra détecter cette maladie orpheline?
Merci à vous
Bonjour Sabrina,
S’agissant d’une maladie auto-immune, elle est détectable grâce au Dpi et peut être évitée.
Passez une bonne journée!
Merci de votre réponse
la drépanocytose peut-elle être éviter grâce au DPI?
Bonjour Gigi,
La drépanocytose est due à une anomalie de l’hémoglobine et est totalement génétique. Cette maladie est effectivement détectable par diagnostic pré-implantatoire.
En France, le DPI est très encadré. Seuls les couples présentant une forte probabilité de donner naissance à un enfant atteint d’une maladie génétique d’une particulière gravité reconnue comme incurable au moment du diagnostic sont autorisés à recourir à ce diagnostic. C’est le cas des couples ayant déjà eu un enfant atteint de drépanocytose ou de couples sans enfants, dont les deux partenaires sont porteurs sains.
Le DPI consiste à rechercher l’anomalie génétique responsable de la maladie sur des embryons obtenus par fécondation in vitro. Cette technique permet de sélectionner les embryons qui n’ont pas l’anomalie génétique pour les implanter dans l’utérus. Elle évite ainsi aux parents d’avoir recours à un diagnostic prénatal, suivi éventuellement d’une interruption médicale de grossesse.
J’espère avoir répondu à votre question.
Bonne journée,
Est-ce que le diagnostic préimplantatoire peut détecter la trisomie 21?
merci pour votre réponse.
Bonjour Eulalie,
En général, selon des facteurs comme l’âge de la patiente, le dépistage permet d’estimer le risque pour une femme enceinte d’avoir un fœtus porteur d’une anomalie génétique telle que la trisomie 21.
Un diagnostic est alors proposé aux femmes à risques. Le diagnostic consiste dans l’analyse des chromosomes du fœtus à partir d’un prélèvement invasif (amniocentèse ou choriocentèse).
Il n’est donc pas pratiqué avant le transfert mais bien une fois le foetus dans l’utérus.
Bon courage,